NOTICIAS
Resumen: VII Congreso de la Sociedad Española de Enfermedad Celiaca

La ciudad de Huesca fue la anfitriona virtual de la séptima edición del Congreso Nacional de la SEEC que supuso una puesta al día de las investigaciones más recientes en el campo de la enfermedad celíaca y la dieta sin gluten, de la mano de figuras científicas destacadas del panorama nacional y con ponentes invitados de Italia, Reino Unido, Estados Unidos y Canadá.
Enfermedad celiaca y COVID-19
La Dra. María Inés Pinto Sánchez (Universidad McMaster de Hamilton, Canadá) fue la encargada de impartir la conferencia inaugural del congreso dedicada a exponer la relación entre la enfermedad celíaca (EC) y la COVID-19. La preocupación inicial surge de la implicación de ciertos virus en la patogenia de la EC, de la mayor vulnerabilidad de algunos pacientes celíacos frente a infecciones víricas y bacterianas (gripe y neumonía) y de la presencia de síntomas digestivos en más de la mitad de las personas afectadas por COVID-19.
A lo largo de la pandemia se han realizado diversos estudios en diferentes países del mundo para conocer si existe un mayor riesgo de contagio con el coronavirus SARS-CoV-2 o de contraer la enfermedad COVID-19 si se padece EC.
El más numeroso y extenso, realizado mediante encuesta online a más de 18.000 personas con y sin EC en 6 países de 3 continentes entre marzo y junio de 2020, concluye que el único factor que incrementa las posibilidades de obtener un resultado positivo al realizarse un test de COVID-19 es haber tenido contacto previo con un caso positivo de COVID-19. Ni la EC ni las enfermedades asociadas a ella de tipo autoinmune, cardiovascular o respiratorio determinan un mayor riesgo de contagio, y tampoco el hecho de hacer bien o mal la dieta sin gluten.
Estudios más limitados llegan a conclusiones similares. En Italia se encuestó telefónicamente a 21 pacientes con EC refractaria y hasta el momento (el sondeo se hizo en abril de 2020) ninguno había contraído COVID-19. Argentina, por su parte, confirmó que esta tónica se mantiene al avanzar la pandemia, tras sondear a 3.500 personas con y sin EC entre octubre y diciembre de 2020.
En cuanto al pronóstico de la COVID-19 en pacientes con EC, Suecia ofrece unos resultados tranquilizadores tras evaluar a más de 224.000 personas afectadas por COVID-19, entre ellas 31.000 con EC. Éstas no presentaron síntomas más severos ni un mayor índice de ingreso hospitalario que las que no padecían EC, concluyendo que la gravedad o el riesgo de complicaciones de la COVID-19 no es mayor en personas con EC. No obstante, permanece abierto un registro internacional para conocer la evolución de las personas celíacas que hayan sufrido COVID-19. Se trata del proyecto SECURE-Celiac, liderado por la Universidad de Columbia, en Nueva York, y destinado a los médicos que atienden a pacientes afectados por ambas enfermedades.

En cuanto al acceso a los productos sin gluten durante el confinamiento, una encuesta belga realizada con 100 pacientes con EC concluye que fue más difícil conseguir este tipo de productos, y en Italia, de los casi 2.000 encuestados, un tercio afirmaba haber tenido más dificultades para conseguir productos específicos sin gluten, pero a la vez un tercio reconoció que había podido seguir una dieta sin gluten más estricta.
Y en relación con la percepción del riesgo, entre las 276 personas encuestadas en las regiones italianas de Salerno y Padua, las personas ancianas, las mujeres y los afectados por otras patologías además de la EC fueron los que mostraban mayor preocupación por la pandemia. A la mitad le preocupaba especialmente el contagio y hasta un 60% era extremadamente vigilante con las medidas frente al contagio.
En línea con lo anterior, un estudio multicéntrico con 10.700 personas celíacas encuestadas entre abril y junio de 2020 mostró que un 25% percibía un mayor riesgo de contraer infecciones en general, un 60% sentía un mayor riesgo de contraer COVID-19 y hasta un 70% se quejaba de falta de información, que obtenían de internet (30%) asociaciones de pacientes (30%) o de los médicos (10%). Un 30% aseguraba extremar la vigilancia para prevenir el contagio.
Y finalmente, sobre las vacunas frente a COVID-19 poco que decir, pues no se han hecho estudios específicos en personas con EC.
Enfermedad celíaca en niños y adolescentes
En el apartado pediátrico, la Dra. María Roca (Hospital La Fe, Valencia) centró su intervención en el análisis de péptidos tóxicos de gluten (GIP, Gluten Immunogenic Peptides) en heces y orina para el control de los pacientes diagnosticados de enfermedad celíaca (EC). Este método es revelador ante el hecho de que en ocasiones las transgresiones dietéticas no provocan síntomas ni elevación de anticuerpos en sangre ni son detectadas mediante los cuestionarios dietéticos. Y son muy útiles para averiguar si en los casos en los que persisten los síntomas o los anticuerpos elevados la causa es la ingesta inadvertida de gluten.
Los estudios realizados en menores muestran que el porcentaje de transgresiones dietéticas aumentan con la edad, siendo especialmente relevantes en la adolescencia y en familias con padres peor informados. También reflejan cierta relajación tras los 6 meses posteriores al diagnóstico. El análisis de GIP en heces muestra que en el momento del diagnóstico prácticamente todos pacientes ofrecen un resultado positivo (entre el 95% y el 97%, según los estudios), a los 6 meses se sigue detectando gluten en el 13-17% de los casos, pero al cabo de un año el porcentaje de pacientes que ingieren algo de gluten sube hasta el 25-27%.
Este hecho se corrobora en un estudio de la Dra. Roca, en el que al analizar las heces de niños y adolescentes que llevan entre 6 meses y 15 años haciendo dieta sin gluten detecta gluten en el 35% de ellos, muchos de los cuales pensaban que hacían correctamente la dieta sin gluten ante la ausencia de síntomas o anticuerpos en sangre.
Los estudios que han utilizado estos métodos han podido comprobar también que existe una correlación entre la cantidad de gluten ingerido y la cantidad de gluten (GIP) detectado en las heces, aunque con gran variabilidad entre individuos, y que en los 2 primeros días tras el inicio de la dieta sin gluten se produce una caída abrupta en la cantidad de gluten detectado en las heces, y a partir de ahí el descenso es mucho más suave y estable.
Queda por definir el protocolo más adecuado para la toma de muestras (cuáles, cuántas y cada cuánto tiempo) y las situaciones en las que sería recomendable hacer este análisis. La Dra. Roca sugiere tomar 2 ó 3 muestras en días alternos tratando de que al menos una sea en fin de semana; en bebés prefiere muestras de heces y en niños más mayores muestras de orina.
La Dra. María Luisa Mearin (Centro Médico Universitario de Leiden, Países Bajos) habló sobre el seguimiento de los pacientes planteando algunas paradojas. Por un lado, existen guías muy buenas y completas para el diagnóstico de la EC, sin embargo, casi no hay guías para el seguimiento, a pesar de tratarse de una enfermedad crónica con un tratamiento de por vida que debe ser vigilado. Por otro lado, los controles que se realizan habitualmente a los pacientes, que son trimestrales durante el primer año tras el diagnóstico y después anuales, además de la evaluación del estado general de salud, síntomas, crecimiento (peso y talla) y de la dieta sin gluten, incluyen una batería de pruebas de laboratorio (anticuerpos, vitaminas, minerales, función tiroidea, etc.) que son siempre normales en los pacientes ya recuperados y por tanto podrían ser prescindibles.
Se echa de menos, en cambio, preguntar al niño cómo se encuentra, y valorar su calidad de vida con cuestionarios específicos diseñados para tal fin, junto con cuestionarios dietéticos encaminados a detectar errores en la dieta sin gluten o malos hábitos de alimentación, todo ello mucho más fácil ahora que se ha normalizado el uso de herramientas online. Incluso el control analítico de anticuerpos podría realizarse en casa con los tests rápidos que ya existen, y podrían incorporarse igualmente a estos controles el análisis de gluten en heces u orina en sus versiones domésticas, también disponibles.
Los sondeos que realiza la Sociedad Europea de Gastroenterología, Hepatología y Nutrición Pediátrica (ESPGHAN) entre los profesionales de esta especialidad en Europa revelan, por ejemplo, que un 35% de los especialistas nunca evalúan la calidad de vida de sus pacientes celíacos, o que el 11% de ellos sólo controlan la EC con un análisis serológico de anticuerpos. En cuanto a los recursos profesionales de los centros, el 25% no disponen de dietista-nutricionista y el 35% carecen de atención psicológica, a la que recurren y costean por su cuenta en torno al 20% de los pacientes.
Un caso especial que también se abordó en este congreso fue la EC potencial, definida en pediatría como la elevación de autoanticuerpos en sangre (antitransglutaminasa o antiendomisio) en ausencia de atrofia de vellosidades intestinales, existiendo predisposición genética para la EC (HLA DQ2 y/o DQ8), con o sin síntomas de la enfermedad. Es una situación que puede evolucionar hacia una EC activa con atrofia de vellosidades (lesión Marsh tipo 3) o bien revertir espontáneamente a pesar de seguir haciendo dieta normal con gluten, según expuso la Dra. Renata Auricchio (Universidad Federico II de Nápoles, Italia).
En un grupo de 340 pacientes pediátricos diagnosticados de EC potencial y estudiados por la Dra. Auricchio, 60 presentaban síntomas e iniciaron la dieta sin gluten. El resto, al ser asintomáticos, permanecieron consumiendo gluten para analizar su evolución. 39 desarrollaron síntomas con posterioridad y también comenzaron la dieta sin gluten. Otros 42 iniciaron igualmente la dieta porque se vio que habían desarrollado atrofia de vellosidades en una de las biopsias periódicas de control a las que eran sometidos los participantes. Pero 166 permanecieron en el estado potencial y sin síntomas al cabo de varios años a pesar de seguir consumiendo gluten, con unos niveles de anticuerpos en sangre que se mantuvieron positivos en el 43% de los casos, desaparecieron en el 20% y fluctuaron entre valores positivos y negativos en el 37% restante.
Se comprobó que es más probable que la EC potencial derive en una EC activa cuando los pacientes tienen más de 10 años, tienen lesión Marsh tipo 1 en el intestino (linfocitosis intraepitelial sin atrofia) y sus anticuerpos permanecen elevados en sangre a lo largo del tiempo. Así, es posible predecir correctamente qué pacientes potenciales van a desarrollar finalmente la EC activa en el 80% de los casos, o en el 87% si se trata de casos que llevan más de dos años con anticuerpos antitransglutaminasa elevados.
Cuando la EC potencial va acompañada de síntomas, los más habituales son el bajo peso (36% de los casos), el dolor abdominal (34%) y la diarrea (19%), los cuales persisten después de un año de dieta sin gluten en casi la mitad de los casos.
Para cerrar este bloque, la Dra. Auricchio expuso otras causas que pueden provocar atrofia de vellosidades y dar lugar a falsos diagnósticos de EC, aunque sólo representan el 5% de los casos de atrofia, entre ellas las alergias alimentarias, el reflujo gastroesofágico, la enfermedad inflamatoria intestinal, el síndrome de intestino corto o la diarrea congénita.
Enfermedad celíaca en adultos
El Dr. Miguel Montoro (Hospital San Jorge, Huesca) inició este apartado refiriéndose a la enfermedad celíaca (EC) seronegativa, es decir, a los casos de EC en los que existe atrofia de vellosidades pero no hay elevación de los anticuerpos específicos en sangre. Es poco frecuente, un estudio italiano detectó sólo 14 casos de EC seronegativa en un grupo de 840 pacientes adultos diagnosticados de EC. Por su parte, entre todos los casos de atrofia seronegativa, la EC es la causa más frecuente, aunque sólo está detrás del 30% de ellos, siendo el 70% restante debido a otros motivos, como el sobrecrecimiento bacteriano, la infección con parásitos (principalmente Giardia), enteropatías autoinmunes, enteritis eosinofílicas o el consumo de ciertos fármacos, como el antihipertensivo Olmesartán. Además, un porcentaje de casos de atrofia seronegativa no tiene identificada su causa y se resuelve espontáneamente sin retirar el gluten de la dieta. Para evitar errores de diagnóstico y la prescripción innecesaria de la dieta sin gluten es muy importante asegurar que la atrofia seronegativa es realmente debida a la EC, y para ello se hace necesario confirmar que el paciente tiene predisposición genética a EC (HLA DQ2 y/o DQ8), que el análisis de anticuerpos que ha resultado negativo se realizó cuando el paciente aún consumía gluten, que otras posibles causas de atrofia han sido descartadas y que la lesión intestinal se resuelve al hacer la dieta sin gluten.
Otro de los retos diagnósticos que se dan en la edad adulta tienen que ver con la persistencia de la atrofia de vellosidades a pesar de la dieta sin gluten, que puede deberse a un diagnóstico erróneo de la EC o a un mal cumplimiento de la dieta sin gluten o a la temida EC refractaria. Según expuso el Dr. Fernando Fernández Bañares (Hospital Mutua Terrassa, Barcelona), hasta un 62% de los adultos diagnosticados de EC siguen con atrofia de vellosidades tras 2 años de dieta sin gluten, y entre los factores implicados en esta lenta recuperación figuran la edad del paciente, el tiempo transcurrido desde el diagnóstico y el grado de adherencia a la dieta sin gluten. Éste último es un factor clave, porque la ingesta accidental de gluten no siempre provoca síntomas y no suele ser detectada por las encuestas dietéticas que persiguen identificar este tipo de errores, a lo que se suma la percepción subjetiva de hacer correctamente la dieta sin gluten. Incluso los anticuerpos específicos de EC antitransglutaminasa y antiendomisio se mantienen en valores negativos en la mitad de los casos en los que persiste la atrofia, según revela el análisis de gluten en heces. Por estos motivos se hace necesario valorar la pertinencia de hacer al menos una biopsia de seguimiento al cabo de 1 ó 2 años del diagnóstico en adultos, especialmente si presentaban cuadros digestivos graves en el momento del diagnóstico o sus síntomas no terminan de resolverse.
Para tratar estas situaciones se investigan fármacos que eviten las consecuencias de ingestas accidentales de gluten, y de ello habló el Dr. Francisco León (compañía farmacéutica Provention Bio Inc., Nueva Jersey, Estados Unidos). Lo primero que destacó es la importancia de diferenciar entre la EC que no responde a la dieta sin gluten por los motivos indicados anteriormente (afecta al 30% de los pacientes adultos) y la EC refractaria, una complicación grave de la EC, que se mantiene activa a pesar de hacer correctamente la dieta sin gluten. Afecta al 1% de casos de EC. Se caracteriza por la presencia de linfocitos intraepiteliales aberrantes en las biopsias de duodeno, que permiten distinguir entre la EC refractaria tipo 1, cuando no superan el 20%, y la EC refractaria tipo 2, cuando hay más de un 20%. Esta situación deriva en un linfoma intestinal de células T en la mitad de los casos y su pronóstico es grave.
La interleuquina 15 (IL-15) es un mediador inmunológico clave en la EC y también en la EC refractaria y centra las investigaciones del Dr. León, quien después de pasar por varias compañías farmacéuticas fundó la empresa Celimmune para adquirir los derechos de un fármaco experimental, AMG714, que había sido desarrollado por la compañía Amgen para tratar la artritis reumatoide y lo abandonó al no cumplir sus expectativas. AMG714 es un anticuerpo monoclonal que bloquea la acción de la IL-15 y fue el motivo por el que se postuló como candidato para tratar la EC. Fue ensayado con relativo éxito en pacientes con EC refractaria tipo 2 y ha sido autorizado para uso compasivo, la compañía lo ofrece sin coste.
En este momento, el Dr. León dirige una nueva compañía, Provention Bio, que se unió a Amgen tras haber ésta adquirido previamente a Celimmune. Está ensayando este fármaco, ahora denominado PRV-015, en pacientes adultos con EC que no responden a la dieta sin gluten pero que no padecen EC refractaria. Pretende evaluar si es capaz de neutralizar las ingestas accidentales de gluten que se pueden producir en el día a día de los pacientes y la administración consistiría en una inyección al mes en el ámbito doméstico. En España se han iniciado en junio los ensayos clínicos en fase 2 con este fármaco experimental y ya se están reclutando pacientes en los 9 hospitales adheridos al ensayo en nuestro país. Participan también Estados Unidos, Canadá y Países Bajos.
Anemia y déficit de hierro en enfermedad celíaca
La anemia ferropénica, causada por un déficit de hierro, y el déficit de hierro sin anemia (ferropenia) son problemas bastante comunes en la enfermedad celíaca (EC) y pueden ser indicio de una EC no detectada. De hecho, la EC se incluye entre las causas que pueden provocar esta anemia, junto con la cirugía bariátrica, la gastritis autoinmune o la presencia de Helicobacter pylori.
En su intervención para abordar este tema, el Dr. Miguel Montoro (Hospital San Jorge, Huesca) indicó que la EC está presente en el 5% de los casos de anemia ferropénica sin síntomas digestivos, en el 13% cuando existen síntomas digestivos y en el 30% si los síntomas digestivos son serios. Por su parte, entre un 12% y un 80% de las personas celíacas muestran anemia en el momento del diagnóstico, según diversos estudios.

El origen del déficit de hierro y de la anemia no está del todo claro y puede no ser debido a un problema de absorción intestinal, pues existen casos de anemia que persiste a pesar de administrar hierro por vía oral en pacientes que ya no muestran lesión intestinal (Marsh 0), independientemente de si tienen o no anticuerpos en sangre.
Se vincula en estos casos la anemia ferropénica con el déficit de vitaminas del grupo B. El 20-30% de los pacientes celíacos con anemia tienen también déficit de ácido fólico (vit. B9), y el 8-41% tienen déficit de vitamina B12. También se consideran, como posibles causas de anemia, la enfermedad inflamatoria intestinal, el sobrecrecimiento bacteriano (SIBO) y el déficit de cobre.
La existencia de anemia ferropénica en el momento del diagnóstico de la EC se asocia con un estado avanzado de la enfermedad y con una respuesta más lenta a la dieta sin gluten. Los pacientes en esta situación suelen tener valores más altos de anticuerpos en sangre y un volumen corpuscular medio más bajo en las analíticas de sangre, así como bajo peso y mayor sensación de fatiga.
Lo esperable es que la anemia se resuelva con la dieta sin gluten. Si no es así, el Dr. Montoro recomienda administrar hierro endovenoso para evitar que el tratamiento con hierro oral sea infructuoso, sobre todo en los pacientes que comenten transgresiones, los que responden lentamente a la dieta sin gluten o los afectados por condiciones inflamatorias o EC refractaria.
Manifestaciones neurológicas en enfermedad celíaca
Es conocido que la enfermedad celíaca (EC) se puede presentar con síntomas extradigestivos, en ocasiones como única manifestación de la enfermedad, y en muchos casos se trata de problemas neurológicos. Igualmente, las alteraciones neurológicas pueden aparecer en respuesta al consumo de gluten en ausencia de EC, por lo que frecuentemente se habla de trastornos neurológicos relacionados con el gluten sin especificar si se trata de EC o de sensibilidad (o intolerancia) al gluten no celíaca (SGNC). Uno de los mayores expertos en este campo es el Dr. Marios Hadjivassiliou (Hospital de Sheffield, Reino Unido), que comenzó su intervención remarcando la utilidad de los anticuerpos antigliadina en estos pacientes, ya que si bien están descatalogados para el diagnóstico de la EC por su baja especificidad (son positivos en el 12% de los sujetos sanos), pueden ser útiles en pacientes con trastornos neurológicos de causa no identificada en los que se sospecha la implicación del gluten, ya que hasta un 41% de pacientes con trastornos neurológicos relacionados con el gluten tienen elevados estos anticuerpos, siendo normales el resto de marcadores.

Es reseñable la mejoría que experimentan estos pacientes al hacer la dieta sin gluten, y el problema neurológico más destacado es la ataxia (denominada ataxia por gluten en este contexto), un trastorno progresivo de la marcha y coordinación motora que no revierte, pero sí frena, su avance una vez retirado el gluten cuando es ésta proteína la causante del problema. También es común la neuropatía periférica, que afecta a la sensibilidad de las extremidades y se presenta hasta en un 21% de pacientes con EC, también en muchos casos de SGNC. Independientemente de si existe o no lesión intestinal, mejora tras un año de dieta sin gluten. El gluten es, de hecho, el responsable del 26% de los casos de esta neuropatía. Y cabe destacar aquí la encefalopatía por gluten, que se manifiesta con dolores de cabeza similares a la migraña que suelen ir acompañados de ‘mente nublada’ y cierta confusión mental. Se da en el 26% de los casos de EC y en el 75% de ellos se resuelve por completo con la dieta sin gluten.
Para concluir, el Dr. Hadjivassiliou retomó el tema de los marcadores serológicos para comentar que si el marcador estrella en la EC es la transglutaminasa tisular (o transglutaminasa 2, TG2), y en la dermatitis herpetiforme es la transglutaminasa epidérmica (TG3), en la ataxia por gluten es la transglutaminasa neuronal (TG6), cuya valoración de rutina está disponible en el Hospital de Sheffield desde 2019 (antes sólo estaba en uso en el ámbito de la investigación). Según sus datos, este marcador es positivo en el 96% de los pacientes neurológicos con anticuerpos antigliadina positivos, en el 74% de las ataxias de causa no identificada, en el 53% de los pacientes con EC y en el 4% de la población sana.
Problemas con el diagnóstico de la enfermedad celíaca
Los principales problemas de diagnóstico de la enfermedad celíaca (EC), tal como relató el Dr. Benjamin Lebwohl (Universidad de Columbia, Nueva York, Estados Unidos) son los falsos positivos (casos sin la enfermedad diagnosticados como enfermos), los falsos negativos (casos con la enfermedad diagnosticados como sanos) y, sobre todo, el infradiagnóstico (casos de la enfermedad no detectados).
Los motivos del infradiagnóstico pueden ser varios, pero destaca la falta de sospecha clínica, que lleva a no hacer las pruebas de diagnóstico a las personas afectadas, que van a arrastrar la enfermedad durante años sin ser detectadas. Resulta sorprendente que en muchos casos se realizan endoscopias en pacientes con pérdida de peso, diarreas, anemia o reflujo y no se toman biopsias duodenales porque no se sospecha EC, desaprovechando así la oportunidad de detectar posibles casos ocultos. No son pocos los pacientes que son finalmente diagnosticados de EC después de haberse sometido a una o más endoscopias a lo largo de su vida en las que no se tomaron biopsias y se buscaba otro tipo de problemas que son mucho menos frecuentes.
Y en ocasiones sí se toman biopsias, pero insuficientes para obtener resultados fiables y concluyentes. En la práctica habitual se toman 2 biopsias, cuando lo recomendable es tomar al menos 4 para asegurar que al menos una de las muestras presente claramente una lesión compatible con la EC que pueda ser evaluada. A ello se suma la subjetividad de los patólogos a la hora de evaluar las muestras, lo que origina que una misma muestra puede dar lugar a diferentes diagnósticos según quién la evalúe. El mayor grado de concordancia se suele dar en los centros hospitalarios, pero cuando se evalúa en centros sanitarios de menor nivel o en laboratorios externos las discrepancias son mayores.

Para salvar estas limitaciones, se empieza a debatir ahora la posibilidad de diagnosticar la EC sin biopsia en adultos, siguiendo los criterios que se aplican en pediatría desde hace una década, según los cuales una elevación de anticuerpos IgA antitransglutaminasa 10 veces por encima del valor de corte, junto con valores positivos de anticuerpos IgA antiendomisio, permiten diagnosticar la EC con total fiabilidad. Está comprobado que cumpliéndose ambos criterios, siempre existe atrofia de vellosidades y predisposición genética.
Un estudio reciente realizado en 11 centros de Estados Unidos para evaluar este aspecto muestra que el 29% de los pacientes adultos con EC, 42 en total, presentaban anticuerpos IgA anti-TG2 10 veces por encima del valor normal, y de ellos 40 (un 95%) tenían atrofia de vellosidades en la biopsia de duodeno.
El análisis serológico, no obstante, también plantea sus problemas. Según el Dr. Lebwohl, la valoración de anticuerpos IgA o IgG antipéptidos deamidados de gliadina (DGP) puede dar lugar a un sobrediagnóstico de la EC, y la ausencia de anticuerpos en sangre cuando se observa atrofia de vellosidades intestinales debe llevar a plantearse si se trata de EC seronegativa o de otro problema de salud que no tiene nada que ver. El diagnóstico de EC se verá reforzado si existe predisposición genética (HLA DQ2 y/o DQ8) y si existe mejoría al hacer la dieta sin gluten. La explicación a los valores negativos de anticuerpos puede ser que el paciente ya estaba a dieta sin gluten cuando se realizó la analítica o que habitualmente consume poco gluten porque convive con una persona celíaca.
Alimentación sin gluten
La enfermedad celíaca (EC) puede llevar aparejados ciertos déficits nutricionales antes del diagnóstico, generalmente de minerales como el hierro o el calcio y de vitaminas del grupo B como el acido fólico (B9) o la vitamina B12, a causa de la malabsorción intestinal. Sin embargo, tras el diagnóstico pueden surgir otros desequilibrios nutricionales asociados a la dieta sin gluten. La Dra. Edurne Simón (Universidad del País Vasco, Bilbao) destacó la ingesta excesiva de grasas y proteínas, y deficitaria de hidratos de carbono y fibra, tras el estudio de composición corporal y estado nutricional de más de 200 pacientes con EC evaluados durante la última década.
La versión sin gluten del grupo de alimentos basados en cereales, que suponen el 24% del aporte energético diario, está detrás del exceso de energía, grasa y azúcares simples, y del déficit de proteínas, fibra y micronutrientes, en las dietas sin gluten, al tratarse de productos procesados y ultraprocesados cuya calidad nutricional dista de sus equivalentes con gluten. Hay que recordar que eliminar productos basados en trigo, cebada y centeno supone una reducción drástica en la ingesta de hidratos de carbono y fibra que no llega a ser compensada por el mayor consumo de legumbres que se suele recomendar a las personas con EC. No obstante, en los últimos años ha ido mejorando su formulación, aumentando el aporte de fibra, reduciendo la cantidad de azúcar y proporcionando un perfil lipídico más adecuado.
En ello coincide el Dr. Manuel Gómez Pallarés (Universidad de Valladolid), quién relató que las demandas históricas de las personas celíacas eran primero que hubiese productos sin gluten, después que fuesen buenos y baratos, y por último que fueran sanos. Por ello, las harinas de arroz o maíz y los almidones de maíz, tapioca o patata han dado paso a otros cereales sin gluten (mijo, sorgo, teff) y pseudocereales (trigo sarraceno, amaranto, quinoa), más nutritivos, pero también más caros y con peor sabor y calidad sensorial. Y para emular las propiedades de viscosidad y elasticidad que aporta el gluten es frecuente recurrir a componentes como la goma xantana o la hidroxiprolilmetilcelulosa (HPMC), que proporcionan esponjosidad y cremosidad a los productos que los contienen, así como a goma guar, pectinas, emulgentes, goma de garrofín o carboximetilcelulosa (CMC) como espesantes y estabilizantes.
Más recientemente se van incorporado en las formulaciones de productos sin gluten el almidón de trigo (sin gluten), que aporta mejor sabor, la harina de avena (no contaminada), también con más sabor, más nutritiva y con importante aporte de beta glucanos, y el psyllium, que se obtiene de la cáscara de las judías y tiene propiedades similares a la goma xantana.
La biotecnología ofrece, sin embargo, nuevas estrategias para lograr productos aptos para celíacos. Si lo mencionado anteriormente parte de materias primas sin gluten para elaborar productos gluten-free, la eliminación de gluten en las harinas de cereales con gluten, o la eliminación del gluten en la propia planta darían lugar a productos gluten-safe. Esta última opción es la que abordó la Dra. Susana Sánchez (Instituto de Agricultura Sostenible del CSCI, Córdoba). Su trabajo se centra en preservar las propiedades tecnológicas del gluten de trigo eliminando por ingeniería genética sólo aquellas fracciones de gluten que resultan tóxicas para los celíacos, obteniendo así trigos seguros con las cualidades nutricionales del trigo original.
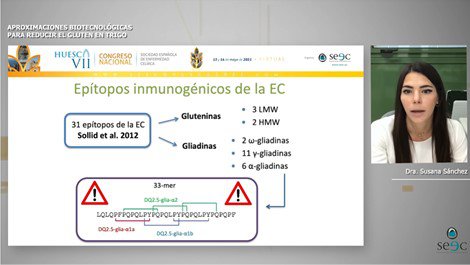
La tarea no es fácil. Las gluteninas, responsables de aportar elasticidad, contienen 5 de los 31 fragmentos tóxicos identificados en el gluten, 2 en las gluteninas de alto peso molecular (HMW) y 3 en las gluteninas de bajo peso molecular (LMW). Las gliadinas, responsables de la viscosidad, albergan los otros 26 fragmentos tóxicos del gluten, 2 en las gliadinas omega, 6 en las gliadinas alfa y 11 en las gliadinas gamma. Y los genes responsables de la expresión de todas estas fracciones de gluten están repartidos por buena parte del genoma del trigo, distribuyéndose en 12 cromosomas y en múltiples copias. Se han identificado 10-15 genes de gliadinas omega, 15-30 genes de gliadinas gamma y 25-150 genes de gliadinas alfa.
La tecnología de ARN interferente permite evitar la expresión de los genes “tóxicos” de forma selectiva impidiendo que el ARN mensajero sea finalmente traducido a proteína. Las variedades de trigo con genes silenciados muestran una reducción en la fracción proteica del grano del cereal, una menor reactividad frente al anticuerpo R5 (el empleado para detectar gluten en alimentos) y una menor capacidad para estimular linfocitos T de pacientes celíacos en ensayos de laboratorio. De hecho, la línea E82 ha permitido elaborar panes de trigo modificado que se han ensayado en pacientes con EC o con sensibilidad al gluten no celíaca y no se ha observado ningún cambio en cuanto a síntomas digestivos ni se han detectado péptidos tóxicos de gluten (GIP, Gluten Immunogenic Peptides) en las heces de los pacientes participantes en el ensayo.
Por su parte, la tecnología de edición génica utiliza el sistema basado en la enzima Cas9 que impide la expresión génica en una etapa incluso anterior, ya que ni siquiera da lugar a la formación del ARN mensajero, al introducir cambios en la secuencia de ADN del gen, desde mutaciones puntuales hasta pérdidas de hasta 100 nucleótidos, que hacen inviable su transcripción. En las líneas de trigo ensayadas con esta tecnología se ha logrado bloquear hasta 35 de los 45 genes de gliadinas alfa presentes (también algunos de gliadinas gamma y omega), con un 75% de muestras mutadas en las que no se ven afectados a nivel fenotípico ni la espiga ni el grano. La reactividad frente a los anticuerpos R5 y G12, que reconocen de forma específica las fracciones tóxicas del gluten, se reduce notablemente, estimándose que han perdido hasta un 85% de su inmunogenicidad (toxicidad).
El papel de la microbiota intestinal
Los estudios más recientes en este campo tratan de establecer la vinculación de los microorganismos intestinales (microbiota intestinal) y su genética (microbioma intestinal) con la función inmunitaria del hospedador y la patogenia de la enfermedad celíaca (EC). El Dr. José Ramón Bilbao (Hospital de Cruces, Barakaldo) recordó que la composición microbiana intestinal de un individuo alcanza el billón de bacterias que suman 1 millón de genes, y que dicha composición varía a lo largo del tiempo. En el caso de la EC, se sabe que existe disbiosis intestinal, con aumento de bacteroides y disminución de bifidobacterias, y que dicha disbiosis precede a la aparición de la EC y persiste tras la instauración de la dieta sin gluten.
La pregunta es si la genética del hospedador influye en su microbiota intestinal y si ésta condiciona la aparición de enfermedades como la EC. Los 57 marcadores genéticos de EC identificados hasta la fecha fuera del sistema HLA (donde residen los marcadores que determinan las variantes ya conocidas DQ2 y DQ8), cuya implicación en el desarrollo de la EC no está aún establecida, centran ahora las investigaciones actuales, que persiguen averiguar si influyen de alguna manera en la microbiota de sus portadores. Se ha comprobado que los sujetos que comparten algunos de estos marcadores de EC tienen una microbiota más parecida.
Asociaciones de este tipo ya conocidas muestran cómo ciertas variantes en el gen de la lactasa se asocian con la presencia de bifidobacterias, o la relación existente entre el sistema de grupos sanguíneos ABO y los bacteroides. En el ámbito de la EC fue descrita la relación entre la variante HLA-DQ2 y una menor proporción de bifidobacterias y más recientemente el grupo del Dr. Bilbao ha revelado que ciertos marcadores genéticos de EC se asocian con cambios en el metabolismo de las bacterias, lo que a su vez se asocia con alteraciones que se dan en el proceso patogénico de la EC. Por ejemplo, un marcador localizado en el cromosoma 22 se asocia con una mayor síntesis de arginina poliamina en las bacterias, lo que favorece el aumento de la permeabilidad intestinal, y otro marcador ubicado en el cromosoma 16 se asocia con una mayor síntesis de lisina en las bacterias, vinculada con una mayor actividad de la enzima transglutaminasa tisular.
Siguiendo con la microbiota intestinal, el Dr. Alberto Caminero (Universidad de McMaster, Hamilton, Canadá) habló del papel de ciertos grupos bacterianos en la patogenia de la EC. Por un lado, hay bacterias que degradan gluten reduciendo su toxicidad, como los géneros Lactobacillus y Rothia, mientras que otras, como la especie Pseudomonas aeruginosa, genera fragmentos con un mayor potencial inmunogénico, incrementando la toxicidad de esta proteína alimentaria. Por otro lado, sabemos que otro componente proteico del trigo, los inhibidores de amilasa-tripsina (ATI), son capaces de activar la inmunidad innata intestinal. En ratones de laboratorio que expresan el marcador humano HLA-DQ8 se ha comprobado que la administración de ATI altera la función de barrera intestinal e induce inflamación, y la administración combinada de ATI y gluten genera, además, enteropatía. La presencia de bacterias del género Lactobacillus capaces de degradar ATI previene este efecto lesivo en el intestino. Otro ejemplo del papel relevante de la microbiota intestinal tiene que ver con el metabolismo del triptófano, un aminoácido presente en muchos alimentos. Existen 3 vías de transformación del triptófano, dos son humanas y una tercera es microbiana. Ésta última está alterada en las personas con EC, y la preponderancia de las dos vías humanas se asocia con una mayor inflamación intestinal (la ruta microbiana libera indoles, que colaboran en la homeostasis).
Simposio de las asociaciones de pacientes
Las 3 asociaciones de pacientes más representativas de nuestro país en cuanto a cobertura geográfica y número de socios contaron por primera vez con un espacio propio en este congreso para mostrar la perspectiva de los pacientes a los médicos e investigadores de la SEEC.
La primera en intervenir fue Ana Campos, de la Federación de Asociaciones de Celíacos de España (FACE), quien habló sobre la normativa de etiquetado que afecta a la alimentación sin gluten. El límite para que un producto sea considerado apto para celíacos fue establecido por primera vez en 1979 por el Codex Alimentarius en su norma CODEX STAN 118/1979 y se fijó en 20 miligramos de gluten por kg de producto. Estos productos no podían contener materias primas o ingredientes derivados de cereales con gluten salvo que hubiesen sido tratadas para reducir su contenido en gluten para no rebasar el límite establecido. El límite de los 20 mg/kg es el actualmente en vigor y está recogido en el Reglamento Europeo 828/2014 para definir los productos “sin gluten”, e incluye también el límite de 100 mg/kg para productos “muy bajo en gluten”. No está regulado el número de controles anuales necesarios para poder hacer estas menciones. Tampoco se regula el uso de pictogramas en los envases.
Por su parte, el Reglamento Europeo 1169/2011 sobre información alimentaria facilitada al consumidor incluye en su artículo 9 las menciones obligatorias, entre ellas las de los 14 alérgenos, que incluyen los cereales con gluten. No quedan definidas, en cambio, las trazas ni la cantidad máxima permitida de cada alérgeno, y esto genera confusión, ya que el etiquetado precautorio exige alegar la presencia de trazas solo cuando ha sido analizada la posible presencia de todos los alérgenos. También inducen a error las alegaciones voluntarias reguladas en el artículo 36, que deben estar basadas en datos científicos y que no deben resultar ambiguas ni confusas, ni inducir a error. Es el motivo por el que un producto que por su naturaleza no puede contener gluten, como un yogur natural, no puede incluir la mención “sin gluten”.
Blanca Esteban, de la Asociación de Celíacos y Sensibles al Gluten de Madrid, expuso los errores más comunes que cometen las personas celíacas a la hora de alimentarse sin gluten en su día a día. El más común es pensar que la mención “sin gluten” significa total ausencia de esta proteína y basar su alimentación en productos manufacturados etiquetados “sin gluten”. Ocurre sobre todo en familias mal informadas, que por lo general no pertenecen a ninguna asociación de pacientes. Las revisiones de dieta de los pacientes que no mejoran sus síntomas o mantienen elevados los anticuerpos en sangre o siguen con lesión intestinal evidencian como fallos más comunes el abuso de productos manufacturados y la compra de productos frescos en lugares poco seguros, como obradores que elaboran a la vez productos con y sin gluten. En el caso de los niños, las transgresiones suelen ocurrir en casa para sorpresa de los padres, que atribuyen el error al comedor escolar. Los adultos, en cambio, transgreden la dieta generalmente fuera de casa y es llamativo que en muchos casos el error es el consumo habitual de cerveza que, a pesar de ser sin gluten, parte de la cebada.
Finalmente, Elisa Mora, de la Asociación Celiacs de Catalunya, habló de las Fake News que afectan al colectivo, expresión que hasta la llegada de Trump a la presidencia de Estados Unidos en 2016 significaba ‘información imprecisa’. Después se ha extendido su uso como sinónimo de desinformación, entendiendo ésta como información manipulada o información para manipular. La ponente expuso como principales mecanismos de desinformación el uso de datos inflados, la generalización a partir de casos particulares, la exposición de datos sacados de contexto, la alusión sesgada sólo a las fuentes que apoyan las tesis del que informa, la información basada en opiniones o ligada a intereses económicos o de otro tipo, así como falsas correlaciones causa-efecto.
Autor: Juan Ignacio Serrano Vela. Doctor en Biología.
Servicio de Investigación y Formación. Asociación de Celíacos y Sensibles al Gluten. Madrid.